W pierwszym etapie produkcji leku wytwarzane są substancje czynne o określonym działaniu farmakologicznym. Jest to zwykle proces tzw. wsadowy, realizowany zgodnie z określoną procedurą. Na przykład antybiotyki na skalę przemysłową wytwarza się podczas fermentacji. Proces ten rozpoczyna się od wprowadzania wyselekcjonowanych kultur mikroorganizmów do specjalnej pożywki.
Zawiera ona różne substancje odżywcze (m.in. źródła laktozy, glukozy i azotu), dzięki którym drobnoustroje szybko się rozmnażają, produkując duże ilości substancji bakteriobójczych. Fermentację przeprowadza się w zbiornikach z mieszadłami, do których doprowadzane jest wysterylizowane i odfiltrowane powietrze oraz środki zapobiegające tworzeniu się piany.
W miarę potrzeb uzupełnia się też pożywkę fermentacyjną. Po pewnym czasie z tej ostatniej trzeba wyizolować oraz oczyścić antybiotyk. Stosuje się w tym celu różne metody.
W wypadku antybiotyków rozpuszczalnych w wodzie jest to zwykle wymiana jonowa, natomiast substancje rozpuszczalne w olejach, m.in. penicylinę, oczyszcza się w procesie ekstrakcji rozpuszczalnikowej. Ostatecznie uzyskuje się antybiotyk w proszku.
STEROWANIE PRODUKCJĄ WSADOWĄ

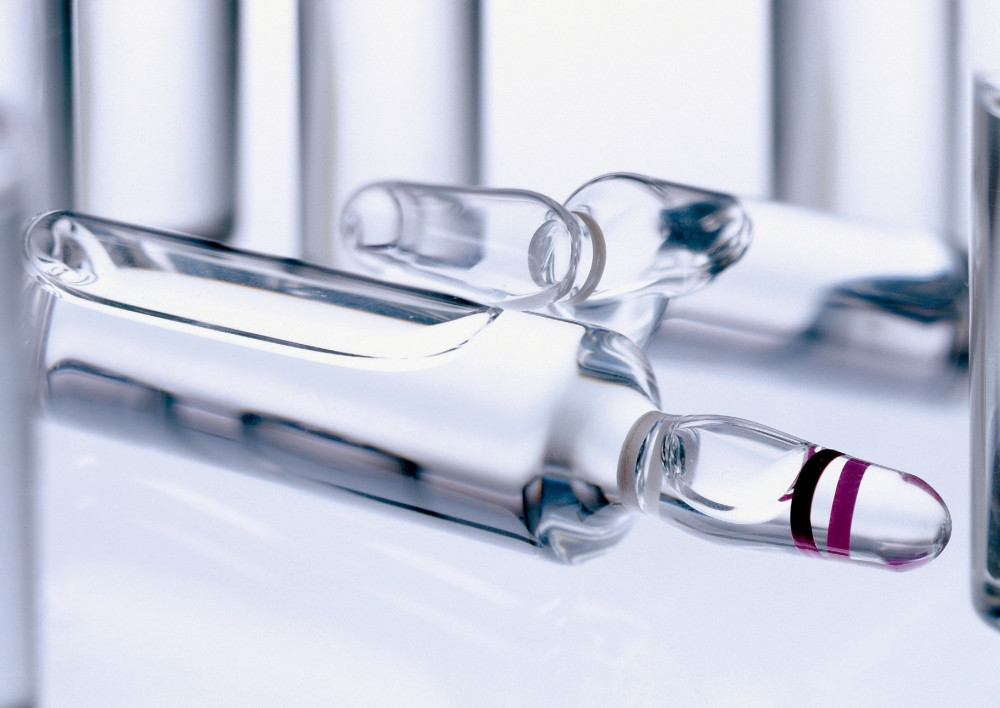
Fot. 1. Liofilizat w fiolkach (źródło: Haupt Pharma)
Produkcją wsadową steruje się za pośrednictwem odpowiednio skonfigurowanej platformy sprzętowo-programowej. Na jakość produktu końcowego oraz sprawność zarządzania procesami tego typu duży wpływ ma używane oprogramowanie (patrz ramka). Powinno się ono charakteryzować skalowalnością oraz zapewniać łatwą integrację z systemem sterowania.
Ponadto zarządzanie recepturami (dodawanie nowych, ich usuwanie oraz edycja) musi być maksymalnie uproszczone. Czynności te nie mogą też wpływać na przebieg realizowanych zadań produkcyjnych. Programowanie takich systemów jest łatwiejsze, jeżeli można tworzyć biblioteki często wykorzystywanych procedur oraz pracować w trybie symulacji (bez połączenia z systemem sterowania).
Z kolei aby zwiększyć ich bezpieczeństwo, dostęp do aplikacji zabezpiecza się hasłem. Fabryki wyrobów farmaceutycznych są często kontrolowane przez różne instytucje nadzorujące bezpieczeństwo oraz jakość leków. W trakcie takiej inspekcji producent jest zobowiązany do okazania na żądanie kontrolerów pełnej historii danej partii produktu.
Stąd możliwość rejestracji takich danych oraz tworzenia z nich tzw. raportów genealogii wsadu również musi być zaimplementowana w oprogramowaniu do zarządzania produkcją wsadową.
Archiwalne informacje o przebiegu produkcji są ponadto przydatne w czasie jej planowania oraz analizy kosztów i wydajności. Najlepiej jeżeli zawartość takich danych można różnicować w zależności od potrzeb różnych odbiorców, na przykład poszczególnych działów zakładu.
MASZYNY SPECJALISTYCZNE
 Kolejnym etapem produkcji jest połączenie substancji czynnych ze środkami pomocniczymi (m.in. laktozą, celulozą, stearynianem magnezu). Te ostatnie nie mają bezpośredniego wpływu na organizm człowieka, a jedynie ułatwiają połykanie lekarstw, poprawiają ich smak lub je konserwują.
Kolejnym etapem produkcji jest połączenie substancji czynnych ze środkami pomocniczymi (m.in. laktozą, celulozą, stearynianem magnezu). Te ostatnie nie mają bezpośredniego wpływu na organizm człowieka, a jedynie ułatwiają połykanie lekarstw, poprawiają ich smak lub je konserwują.
Dalsza obróbka takiej mieszanki zależy od tego, w jakiej postaci (płynnej, półpłynnej, stałej) oraz w jaki sposób lek będzie podawany pacjentom (dożylnie, doustnie, wziewnie, naskórnie). Przykładowo w wypadku tabletek ziołowych rozdrobniony susz roślinny zmieszany z substancjami wiążącymi najpierw waży się i porcjuje.
Następnie masę tabletkową umieszcza się w matrycach prasy, a później gotowe tabletki pakuje do butelek lub blistrów. Składniki lekarstw w płynie i półpłynnych są z kolei najpierw mieszane w specjalnych zbiornikach, skąd są rurociągami pompowane do linii napełniania przykładowo fiolek, ampułek, butelek lub tub.
Do obróbki mieszanki substancji czynnych i pomocniczych wykorzystywane są różne maszyny specjalistyczne, zwykle zautomatyzowane. Przykładem są kapsułkarki, powlekarki, blistrownice, systemy automatycznej kontroli wagi oraz liofilizatory. Te ostatnie służą do suszenia sublimacyjnego. Pierwszym etapem tego procesu jest szybkie zamrożenie roztworu z substancją czynną do bardzo niskiej temperatury, około -100°C.
Następnie umieszcza się go w komorze próżniowej, w której zachodzi proces parowania rozpuszczalnika bezpośrednio z fazy stałej do gazowej. Opary są odprowadzane na zewnątrz, a gotowy liofilizat umieszcza się w fiolkach (patrz fot. 1 i 2) lub formuje w tabletki. Przed użyciem należy go rozpuścić w wodzie. Dzięki liofilizacji można znacznie wydłużyć termin ważności leków.
Kontrola oznaczeń opakowań zapisanych alfabetem Braille'a |
ROBOTY PRZEMYSŁOWE W PRODUKCJI LEKÓW
Z powodu wolumenu oraz szybkości produkcji zautomatyzowane są również zadania transportu oraz pakowania leków. Do tego ostatniego coraz częściej używa się robotów przemysłowych, głównie z powodu ich szybkości oraz powtarzalności.
Ponadto w tym zastosowaniu maszyny te najczęściej współpracują z systemami wizyjnymi, dzięki którym rozpoznają poszczególne produkty na przykład na podstawie kodu kreskowego. Zmniejsza to prawdopodobieństwo pomyłki polegającej przykładowo na umieszczeniu opakowań w nieodpowiednim kartonie.
Stanowiska zrobotyzowane można też łatwo i szybko przeorganizować, podczas gdy personel trzeba najpierw przeszkolić, a później dać mu czas na opanowanie nowych procedur. W przemyśle farmaceutycznym jest to szczególnie cenna zaleta robotów przemysłowych, ponieważ zmiany profilu lub parametrów produkcji są częste.
Jest to na przykład wymagane w sytuacji, gdy hurtownicy zgłoszą zapotrzebowanie na dany produkt w opakowaniach o mniejszej lub większej liczbie tabletek niż dotychczas.
Na stanowiskach, na których pracują roboty, łatwiejsze jest też utrzymanie sterylnych warunków. Dlatego są one na przykład używane w tzw. clean roomach. Roboty w produkcji leków zastępują także ludzi w zadaniach wymagających kontaktu z substancjami szkodliwymi dla zdrowia.
SENSORY
 W obrębie linii technologicznych instaluje się ponadto różne czujniki, za pośrednictwem których zbierane są dane wejściowe systemów sterowania, m.in. robotami, napędami przenośników i dyszami dozowników. Są to na przykład laserowe czujniki odległości.
W obrębie linii technologicznych instaluje się ponadto różne czujniki, za pośrednictwem których zbierane są dane wejściowe systemów sterowania, m.in. robotami, napędami przenośników i dyszami dozowników. Są to na przykład laserowe czujniki odległości.
Wykrywają one obecność obiektów na taśmie (na przykład butelek na tabletki), zliczają je, kontrolują ich położenie (na przykład wkładek w ampułko-strzykawkach) oraz mierzą wielkości geometryczne (przykładowo średnicę bel z folią do pokrywania spodów blistrów). Innym przykładem stosowanych elementów są czujniki kontrastu.
Montuje się je m.in. na linii zgrzewania brzegów tubek z maściami, gdzie ich zadaniem jest określenie współrzędnych specjalnych znaczników naniesionych na tych opakowaniach. Dane te są przesyłane do sterownika zgrzewarki, dzięki czemu informacje nadrukowane na tubie w pobliżu zgrzewu nie ulegają zniszczeniu.
Na zbiornikach z płynnymi składnikami leków montowane są z kolei sensory ultradźwiękowe mierzące poziom ich napełnienia. Zwykle są to dwa czujniki. Pierwszy z nich wykrywa spadek poziomu płynu w zbiorniku do minimum, poniżej którego nie można już zapewnić ciągłości produkcji. Drugi czujnik służy natomiast do detekcji przekroczenia maksymalnej wartości tej wielkości, co grozi przepełnieniem zbiornika.
Niezbędnym elementem wyposażenia linii produkcyjnych w fabrykach leków są ponadto różnego typu czujniki oraz analizatory online do pomiaru takich wielkości jak pH, przewodność cieczy, zawartość rozpuszczonego tlenu, stężenie chloru, temperatura oraz natężenie przepływu.

 Z kolei ręczne pomiary wysokości kropek obarczone są dużymi błędami wynikającymi z różnej siły nacisku poszczególnych operatorów. Ponadto w trakcie badania wypukłości mogą ulec zniszczeniu. Kontrola taka jest także bardzo czasochłonna, przez co nie sprawdza się w produkcji na masową skalę.
Z kolei ręczne pomiary wysokości kropek obarczone są dużymi błędami wynikającymi z różnej siły nacisku poszczególnych operatorów. Ponadto w trakcie badania wypukłości mogą ulec zniszczeniu. Kontrola taka jest także bardzo czasochłonna, przez co nie sprawdza się w produkcji na masową skalę.


























